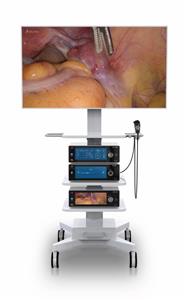
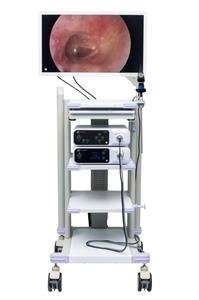
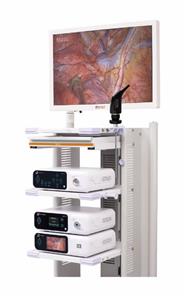
Endoskopik Mukozal Rezeksiyon (EMR) ve Endoskopik Submukozal Diseksiyon (ESD)
Arka plan
Endoskopik mukozal rezeksiyon
Endoskopik mukozal rezeksiyon (EMR), gastrointestinal (GI) sistemin yüzeyel neoplazmalarının evrelenmesi ve tedavisi için kullanılan bir tekniktir. Bu teknik ilk olarak Japonya'da erken mide kanserinin (EGC) tedavisi için geliştirildi ve o zamandan beri displastik Barrett mukozası ve sesil kolon neoplazmaları dahil olmak üzere çeşitli endikasyonlar için tüm dünyaya yayıldı. EMR'nin faydası, aşağıdakileri yapabilme yeteneğine dayanır:
- Yüzeysel GI neoplazmalarının doğru histolojik evrelemesini sağlayın
- Yüzeysel malignitelerin çıkarılması için minimal invaziv bir teknik sağlayın
Şu anda enjeksiyon destekli, başlık destekli ve ligasyon destekli teknikler dahil olmak üzere çeşitli EMR varyasyonları kullanılmaktadır. Hepsi lezyonun tanımlanması ve sınırlarının belirlenmesi, lezyonu kaldırmak için submukozal enjeksiyon ve endoskopik snare rezeksiyonunun temel ilkelerine bağlıdır. Uygun şekilde seçilmiş hasta popülasyonlarında genel güvenliği ve etkinliği sayesinde EMR, yüzeysel GI malignitelerinin tanı ve tedavi algoritmalarına sıkı bir şekilde entegre olmuştur.
Bazı yazarlar, dirençli gastroözofageal reflü hastalığını (GERD) tedavi etmek için antireflü mukozektomi (ARMS) olarak bilinen bir prosedürde EMR'nin kullanımını da incelediler.
Endoskopik submukozal diseksiyon
Endoskopik submukozal diseksiyon (ESD), daha büyük tümörleri rezeke etmek ve EMR ile mümkün olandan daha yüksek en-blok rezeksiyon oranlarının elde edilmesine yardımcı olmak için geliştirilmiştir. ESD'nin temel amacı, bir R0 rezeksiyon elde etmektir. Amerika Birleşik Devletleri'nde, ESD öncelikle bu teknikte deneyimli uzman endoskopistler tarafından belirli merkezlerde gerçekleştirilir. ESD genellikle aşağıdakiler için endikedir: :
- İntramukozal ila yüzeyel submukozal invazyonu olan karsinom olarak teşhis edilen tümörler
- 20 mm'den küçük olsa bile EMR ile çıkarılamayan submukozal fibrozlu lezyonlar
- Bir tuzağın EMR ile başarılı bir en-blok rezeksiyonu sağlama olasılığının düşük olduğu durumlar
- Büyük poliplerin, erken kolorektal kanserin ve majör cerrahi rezeksiyondan kaçınmak isteyen hastalarda transanal yolla ulaşılamayan lezyonların çıkarılması
Lezyonların endoskopik ve ultrasonografik karakterizasyonu
Lenf nodu metastazlarının tahminine yardımcı olabilecek erken GI kanserlerinin evrelemesi için çeşitli sınıflandırma sistemleri geliştirilmiştir. Bu çalışmanın çoğu, EGC'nin evrelemesi ve tedavisi için Japon gastroenterologlar tarafından öncülük edilmiştir. Japon Gastroenteroloji Derneği (JSGE), geniş EGC rezeksiyon veritabanlarından çalışarak lezyonları endoskopik özelliklerine ve zımni mural invazyon riskine göre sınıflandırdı.
2002 yılında uluslararası bir konsensüs toplantısında geliştirilen müteakip Paris sınıflandırması, JSGE sisteminin yapısını yansıtıyordu. Bu sınıflandırmada, yüzeysel (tip 0) lezyonlar polipoid (0-I) ve polipoid olmayan kategorilere (0-II) ayrılır; bunlar ayrıca saplı (0-Ip), sapsız (0-Is), hafif kabarık ( 0-IIa), düz (0-IIb), hafif çökük (0-IIc) veya kazılmış (0-III).
Viyana sınıflandırmasında lezyonlar, invaziv olmayan (düşük dereceli displazi, yüksek dereceli displazi [HGD]) ve invaziv (intramukozal kanser, submukozayı infiltre eden kanser) olmak üzere iki geniş kategoriye ayrılır.
Mukozal tabaka üst, orta ve alt tabakalara ayrılır: m1 (epitel), m2 (lamina propria) ve m3 (muskularis mukoza). Submukoza benzer şekilde üç katmana ayrılır: sm1, sm2 ve sm3. Muskularis mukozanın 500 μm veya daha az altındaki submukozal tümör tutulumu sm1 (yüzeysel) hastalık, 500 μm'yi geçen tutulum ise sm2-3 (derin) hastalık olarak sınıflandırılır. sm1 katmanı ayrıca katman içindeki yanal yayılma temelinde a, b ve c alt katmanlarına bölünür.
Yüksek frekanslı (≥20 MHz) endoskopik ultrasonografi (EUS), ekojeniteleriyle farklılaşan dokuz ayrı katmandan oluşan mukozal duvarın bir görüntüsünü üretir. Mukozal ve submukozal tabakalara lezyon penetrasyonunun derinliğini dikkatlice inceleyerek, lenf nodu metastazı riskini daha kesin bir şekilde belirleyebilir.
EUS, özofagus kanserinin tümör derinliğini ve lenf nodu durumunu doğru bir şekilde teşhis etmede mükemmel bir duyarlılığa ve özgüllüğe sahiptir. ve şu anda mevcut olan en doğru görüntüleme yöntemi olarak kabul edilir. Doğruluğu T1 hastalığı için %75 ila %82, T4 hastalığı için %88 ila %100 ve lenf nodu tutulumu için %72 ila %80 arasında değişmektedir.
Lenf nodu metastazlı özofagus kanserli ve radyolojik olarak N0 olarak evrelenen hastalarda evrelemenin radyolojik ve patolojik korelasyon ile değerlendirildiği bir çalışmada EUS, kontrastlı (CE) bilgisayarlı tomografi (BT) ve pozitron emisyon tomografisi (PET)/BT rapor edilmiştir. hepsinin nodal hastalığı düşük evreleme olasılığı daha yüksekti, PET/CT'nin bunu yapma olasılığı EUS'den daha yüksekti. EUS'nin N0 ve N+ hastalık için doğruluğu, duyarlılığı ve özgüllüğü %55.4, %42.6 ve %75 idi. Lenf nodlarının çoğu (%82) 6 mm'den küçüktü ve mevcut görüntüleme teknikleriyle doğrudan görselleştirmeyi zorlaştırıyordu (muhtemelen radyolojik ve patolojik evreleme arasındaki farklılığın ana nedeni).
Yanlış pozitif EUS görüntüleri peritümöral inflamasyona atfedilirken yanlış negatif evreleme genellikle EUS tarafından saptanamayan tümörün mikroskobik yayılımından kaynaklanır. Erken özofagus tümörlerinin lenf düğümlerinde mikrometastazlar bulunmuştur (bir çalışmada %44'e kadar ). Teknolojinin sınırlamaları nedeniyle, EUS önemli oranda yanlış pozitif ve negatif hastalık oranlarına tabidir; bununla birlikte, EUS ve ardından EMR ve histopatolojik analiz erken özofagus kanseri evrelemesi için standart bakım olmaya devam etmektedir.